Scoperto un nuovo materiale originato da un’esplosione nucleare
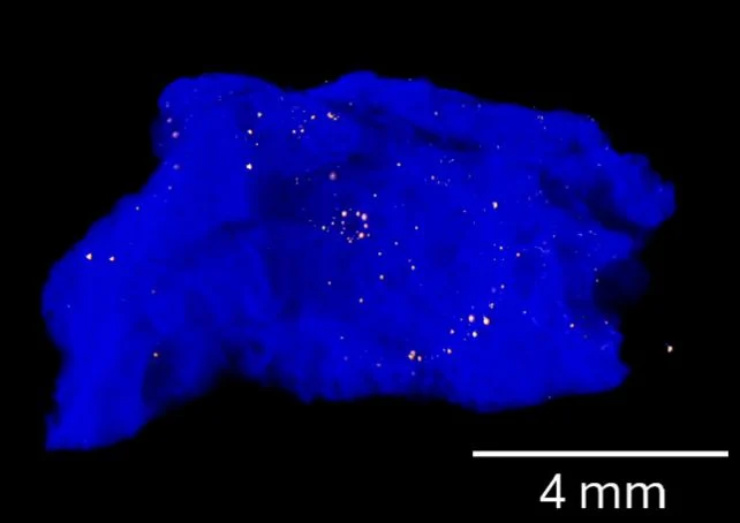
Immagine nano-tomografica del campione di trinitite, con il vetro in blu e le inclusioni di rame in arancione. (Bindi et al., [PNAS])
Un team guidato da Luca Bindi ha identificato nella trinitite rossa del test Trinity 1945 un clatrato di tipo I a base Ca-Cu-Si mai visto prima. Ecco cosa significa per la scienza dei materiali e la sintesi estrema.
Nel luglio del 1945, nel deserto del New Mexico, la prima detonazione nucleare della storia trasformò la sabbia del suolo in un vetro verde-grigiastro che i fisici avrebbero chiamato trinitite. Per decenni questo materiale è stato studiato come curiosità radiologica, reperto storico, oggetto da collezione. Poi, a partire dal 2021, lo stesso campione ha iniziato a restituire qualcosa di molto più inaspettato: strutture cristalline che la chimica convenzionale non aveva mai prodotto, formate in condizioni termodinamiche irriproducibili in qualsiasi laboratorio tradizionale.
La scoperta più recente, pubblicata nel 2025 sul Proceedings of the National Academy of Sciences da un gruppo guidato da Luca Bindi dell’Università di Firenze (con la partecipazione, tra gli altri, di Paul J. Steinhardt di Princeton), riguarda un clatrato di tipo I con formula approssimativa (Ca₃.₃Cu₀.₄Fe₀.₃)Σ₌₄Si₂₃, mai identificato prima in natura né sintetizzato artificialmente. È il primo clatrato confermato cristallograficamente tra i prodotti solidi di un’esplosione nucleare.
La notizia ha una portata che va oltre la fisica atomica o la storia militare. Tocca direttamente la scienza dei materiali, la cristallografia strutturale, la metallurgia estrema e, in modo più sottile ma concreto, la questione di come certi composti possano formarsi (e forse un giorno essere prodotti) a partire da condizioni energetiche che non appartengono all’ordinario.
Cos’è un clatrato e perché questo è diverso da tutti gli altri
Il termine “clatrato” deriva dal latino clathratus, che significa “rinchiuso tra sbarre”. Nella cristallografia dei solidi, un clatrato è un composto in cui una struttura reticolare formata da atomi legati covalentemente crea gabbie poliedriche all’interno delle quali sono intrappolati atomi ospiti. I clatrati di tipo I (la famiglia a cui appartiene quello trovato nella trinitite) hanno una cella unitaria cubica con due tipi di gabbie: dodecaedriche e tetradecedriche, generalmente in rapporto 2:6.
Nella grande maggioranza dei clatrati noti, il reticolo ospitante è fatto di silicio, germanio o stagno, mentre gli ospiti intrappolati sono tipicamente atomi alcalini o alcalino-terrosi, come sodio, potassio, bario e stronzio. La struttura complessiva produce proprietà termoelettriche molto interessanti, tanto che i clatrati di silicio e germanio vengono studiati attivamente come candidati per la conversione di energia termica in elettricità. Questa è la ragione per cui un materiale simile, trovato in una gocciolina di rame intrappolata dentro vetro nucleare, ha suscitato attenzione immediata nella comunità dei materiali.
Il clatrato Ca–Cu–Si della trinitite è però anomalo già nella sua composizione. Il calcio e il rame come elementi che costituiscono il sito ospite (insieme a tracce di ferro) all’interno di un reticolo di silicio non corrisponde a nessuna famiglia sintetica nota. La struttura è stata confermata attraverso la diffrazione di elettroni su singolo cristallo, una tecnica particolarmente adatta per fasi cristalline di dimensioni nanometriche o micrometriche, inaccessibili alla diffrazione X convenzionale su polveri. La determinazione strutturale completa ha richiesto un lavoro di analisi estremamente meticoloso, data la presenza di più fasi cristalline coesistenti nello stesso volume di trinitite rossa.
La trinitite rossa e la storia mineralogica del test Trinity
Non tutta la trinitite è uguale. Il materiale più comune, quello verde pallido che si trova diffusamente attorno al cratere di Trinity, è essenzialmente quarzo fuso e ricristallizzato, contaminato da elementi metallici provenienti dalla torre di detonazione e dai componenti della bomba stessa. La cosiddetta trinitite rossa è molto più rara: si forma nelle immediate vicinanze dell’epicentro, dove le temperature raggiunte nel breve istante dell’esplosione superano ampiamente i 10.000 gradi Kelvin, e il materiale fuso viene a contatto diretto con i vapori metallici (soprattutto rame) provenienti dai cavi elettrici e dai connettori della bomba.
È in queste gocce rossastre, quasi sempre inferiori al millimetro di diametro, che il gruppo di Bindi aveva già identificato nel 2021 un quasicristallo icosaedrico (una struttura a simmetria pentagonale proibita dalla cristallografia classica) a base di silicio, ferro e rame. Quella scoperta era già straordinaria: era il terzo quasicristallo mai trovato in natura (dopo quelli meteorici trovati in Siberia dallo stesso Steinhardt) e il primo prodotto da un evento tecnologico umano.
Il nuovo clatrato è stato trovato nella stessa matrice, nelle stesse goccioline ricche di rame, praticamente adiacente al quasicristallo. Questo non è un caso: entrambe le strutture condividono le stesse condizioni di formazione, ovvero un non-equilibrio termodinamico estremo, con velocità di raffreddamento altissime, pressioni eccezionali e una composizione chimica locale del tutto particolare. Sono, in un certo senso, le due facce di uno stesso evento fisico.
Sintesi in non-equilibrio: cosa cambia rispetto ai processi ordinari
La cristallografia e la scienza dei materiali operano quasi sempre in regime di equilibrio o quasi-equilibrio. Si scaldano miscele a temperature controllate, si mantengono pressioni definite, si raffredda lentamente per permettere alla struttura cristallina di trovare la configurazione a energia minima. In questo modo si ottengono fasi stabili, riproducibili, predicibili. Qualunque fase instabile (cinetica o metastabile) viene normalmente soppressa.
Il test Trinity ha operato in un regime completamente opposto. L’esplosione ha depositato energia in un volume di spazio estremamente piccolo in un tempo dell’ordine dei microsecondi. Le temperature raggiunte erano comparabili a quelle superficiali di una stella. Il successivo raffreddamento è avvenuto altrettanto rapidamente: le gocce di materiale fuso si sono solidificate in un tempo brevissimo, “congelando” strutture che in condizioni normali non avrebbero mai il tempo di formarsi, oppure che, una volta formate, sarebbero immediatamente destabilizzate dal lento raffreddamento verso l’equilibrio.
Questo meccanismo è noto in metallurgia come rapid solidification, ma quello che accade nell’esplosione nucleare va ben oltre i parametri raggiungibili con qualsiasi tecnica industriale di tempra, splat quenching o laser pulse melting. Le velocità di raffreddamento negli esperimenti di sintesi rapida di laboratorio arrivano tipicamente a 10⁶–10⁷ K/s; durante un’esplosione nucleare si stima che le velocità locali possano superare di molti ordini di grandezza questo limite. Il risultato è la stabilizzazione di fasi che appartengono a una sorta di “spazio dei materiali” normalmente inaccessibile.
Implicazioni strutturali: la gabbia di silicio come architettura portante
Dal punto di vista puramente strutturale, il clatrato di tipo I presenta una delle architetture reticolari più eleganti della chimica del solido. Le gabbie poliedriche formate dagli atomi di silicio (con legami Si–Si che richiamano topologicamente le strutture dei fullereni) sono straordinariamente rigide e al tempo stesso capaci di accomodare atomi ospiti di dimensioni molto diverse, con un’interazione guest-host sostanzialmente non covalente. Questo consente di modulare le proprietà del materiale variando il tipo di atomo intrappolato senza modificare la struttura reticolare di base.
Nel caso Ca–Cu–Si, la presenza di calcio e rame come ospiti introduce una complessità chimica non banale. Il calcio è un metallo alcalino-terroso con raggio ionico relativamente grande; il rame è un metallo di transizione con proprietà elettroniche molto diverse. La coesistenza di questi due elementi nelle gabbie dello stesso reticolo (con ferro in tracce) suggerisce che la solidificazione rapida abbia intrappolato una composizione locale del fuso che riflette la miscela di materiali presenti nell’istante dell’esplosione, senza che ci fosse il tempo per una segregazione chimica ordinata.
Questa osservazione apre una questione concettuale importante per la scienza dei materiali computazionale: quanto è affidabile la previsione delle strutture stabili (attraverso metodi come il crystal structure prediction basato su DFT) quando si considerano fasi ottenibili esclusivamente in regime di non-equilibrio? I database di strutture cristalline predette, come quelli generati con USPEX o CALYPSO, operano tipicamente minimizzando l’energia libera in condizioni di equilibrio. Un clatrato Ca–Cu–Si come quello della trinitite non emergerebbe mai da queste previsioni, semplicemente perché non è la fase stabile.
Il contesto mineralogico: trinitite come laboratorio involontario
Guardando la trinitite come oggetto mineralogico, ciò che colpisce è la sua densità di fasi rare per unità di volume. In pochi grammi di vetro nucleare si trovano composti che non si incontrano in nessun altro luogo sulla Terra: oltre al quasicristallo e al clatrato, la trinitite contiene forme di SiO₂ ad alta pressione normalmente associate agli impatti meteoritici, ossidi metallici non stechiometrici, e fasi miste che non corrispondono ad alcuna specie mineralogica ufficialmente classificata.
Questo accumulo di rarità non è casuale. Dipende dalla coesistenza, in un unico evento, di tre condizioni che quasi mai si presentano insieme: temperature elevatissime, pressioni d’urto nell’ordine delle decine di gigapascal, e una composizione chimica molto insolita derivata dalla miscela di sabbia desertica (quarzo, feldspati, argille), metalli del dispositivo di detonazione (rame, ferro, piombo) e materiali della struttura di supporto. Ogni componente di questa miscela ha contribuito alla creazione di un sistema chimico localmente unico, lontanissimo da qualsiasi composizione che si trovi normalmente nella crosta terrestre.
Dal punto di vista della mineralogia descrittiva, la scoperta di Bindi et al. aggiunge una nuova specie potenzialmente approvabile dall’IMA (International Mineralogical Association), sebbene il contesto di formazione artificiale (indotto da attività umana, per quanto involontariamente mineralogica) ponga questioni classificatorie non ancora risolte. La trinitite e i suoi minerali anomali si collocano in una zona di confine tra la mineralogia naturale e quella dei materiali sintetici, un territorio che la comunità scientifica sta imparando a esplorare con strumenti concettuali nuovi.
Caratterizzazione analitica: strumenti e metodi usati
La conferma cristallografica di una nuova fase in un campione complesso come la trinitite rossa richiede una combinazione di tecniche ad alta risoluzione spaziale. Il gruppo di Bindi ha impiegato la diffrazione di elettroni su cristallo singolo con un microscopio a trasmissione (TEM) equipaggiato con un sistema di precession electron diffraction, tecnica che permette di raccogliere dati di diffrazione quasi-cinematici da cristalliti di dimensioni nell’ordine del centinaio di nanometri. L’analisi chimica locale è stata effettuata con spettroscopia a dispersione di energia (EDS/EDX), mentre la mappatura composizionale ad alta risoluzione ha utilizzato STEM-HAADF.
La difficoltà principale non stava nella risoluzione strumentale, ma nell’interpretazione: in un volume così piccolo di materiale vetroso coesistono fasi amorfe, fasi cristalline metastabili, inclusioni metalliche e interfacce discontinue. Separare il segnale del clatrato da quello delle fasi circostanti ha richiesto un lavoro di analisi dei pattern di diffrazione estremamente accurato, supportato da confronti con strutture note di clatrati di silicio e da simulazioni ab initio.
La struttura risultante è stata poi validata tramite raffinamento di Rietveld su dati di polveri, nella misura in cui la quantità di materiale disponibile lo permetteva (quantità minuscole, dato il carattere irripetibile del campione). Ogni frammento di trinitite analizzato è un campione unico, non riproducibile, che rende ogni tecnica distruttiva un costo permanente in termini di perdita di informazione.
Verso la sintesi controllata: cosa insegna la trinitite ai progettisti di materiali
La domanda che inevitabilmente emerge da queste scoperte è se e come un clatrato Ca–Cu–Si possa essere sintetizzato in condizioni controllate. Non esistono oggi metodi standard che raggiungano le velocità di raffreddamento e le temperature dell’esplosione di Trinity. Tuttavia, alcune direzioni sono esplorabili.
La sintesi ad alta pressione, combinata con raffreddamento rapido dal fuso, è già utilizzata per produrre clatrati di tipo I e II a base di germanio e stagno con composizioni inusuali. L’alta pressione favorisce la formazione di strutture ad alta coordinazione che sarebbero instabili a pressione ambiente; il raffreddamento rapido successivo le “congela” prima che possano decadere verso fasi più stabili. Estendere questo approccio al sistema Ca–Cu–Si richiede una mappa di stabilità delle fasi che al momento non esiste.
Una seconda via è quella della sintesi meccanochimica assistita da plasma. Le tecniche di plasma spark sintering (SPS) o di sintesi in arco elettrico permettono di raggiungere velocità di riscaldamento e raffreddamento molto superiori a quelle delle fornaci convenzionali, avvicinandosi (almeno parzialmente) alle condizioni di un non-equilibrio termodinamico pronunciato. Non raggiungeranno mai i 10.000 K dell’esplosione nucleare, ma possono esplorare finestre termodinamiche inaccessibili ai processi tradizionali.
C’è però un aspetto che va considerato con onestà: non è detto che la struttura Ca–Cu–Si trovata nella trinitite sia termodinamicamente metastabile in un senso “pratico”. Potrebbe essere talmente lontana dall’equilibrio da decomporsi rapidamente non appena riscaldata anche a temperature moderate. In tal caso, anche se la si riuscisse a sintetizzare, la sua utilità pratica sarebbe limitata a contesti in cui la stabilità termica non è richiesta, oppure a quei campi (come l’elettronica di potenza criogenica) dove la temperatura di esercizio rimane vicina allo zero assoluto.
Proprietà attese e potenziale applicativo dei clatrati al silicio
I clatrati di silicio di tipo I sono materiali con una struttura elettronica peculiare. A seconda della natura e del numero degli atomi ospiti, possono comportarsi da semiconduttori a gap diretto, da semimetalli, o persino da superconduttori a bassa temperatura. Il caso più noto è quello dei clatrati di bario e silicio (Ba₈Si₄₆) che mostrano superconduttività sotto gli 8 K, un valore modesto ma significativo per una struttura a base di silicio puro.
Le proprietà termoelettriche sono forse ancora più interessanti. La struttura a gabbia dei clatrati crea un meccanismo detto “rattling” (letteralmente “ciondolamento”) degli atomi ospiti, che vibrano quasi indipendentemente dalla struttura reticolare rigida circostante. Questo disaccoppiamento produce bassissima conducibilità termica del reticolo, mantenendo al tempo stesso conducibilità elettrica decente: la combinazione ideale per un materiale termoelettrico efficiente. Il parametro di figura di merito ZT, che misura questa efficienza, ha valori promettenti in diversi clatrati sintetici.
Se il clatrato Ca–Cu–Si potesse essere stabilizzato e prodotto in quantità sufficienti, le sue proprietà andrebbero investigate sistematicamente. La presenza di rame (un metallo di transizione con elettroni d parzialmente occupati) potrebbe alterare significativamente il comportamento elettronico rispetto ai clatrati con ospiti puramente ionici. La presenza di calcio, con la sua configurazione elettronica da metallo alcalino-terroso, introduce invece un’ulteriore variabile nella densità di stati vicino al livello di Fermi. Questo cocktail di elementi potrebbe produrre un comportamento elettronico non banale, con accoppiamenti spin-orbita o correlazioni elettroniche che vanno ben oltre la fisica di un semplice clatrato alcalino-terroso.
Il significato del ritrovamento nel quadro più ampio della mineralogia da impatto e da evento estremo
La geologia degli impatti meteoritici ha da tempo dimostrato che eventi di alta pressione e alta temperatura (anche se di brevissima durata) producono fasi mineralogiche che non si trovano in nessun altro contesto geologico. La stishovite e la cosite, due polimorfi del quarzo ad alta pressione, furono identificate per la prima volta nei crateri da impatto prima di essere sintetizzate in laboratorio. Il diamante di lonsdaleite, con struttura wurtzite, viene trovato nei meteoriti e nei siti di impatto; la sua sintesi artificiale è ancora oggetto di discussione.
La trinitite si inserisce in questo schema come un caso limite: non un impatto naturale, ma un evento energetico artificiale che ha replicato (in un volume minuscolo e per un istante brevissimo) le condizioni di un impatto cosmico. Non è una coincidenza che proprio la stessa mineralogia anomala (quasicristalli, strutture ad alta pressione, fasi metastabili) si trovi sia nei crateri di impatto che nella trinitite. Il meccanismo fisico è analogo: shock termico e barico di brevissima durata, con solidificazione rapida del materiale fuso.
Questo parallelismo ha una conseguenza metodologica importante: i mineralogisti che studiano i crateri da impatto potrebbero trovare nei metodi di analisi sviluppati per la trinitite (diffrazione elettronica ad alta risoluzione, mappatura STEM-EDS su cristalliti nanometrici, raffinamento strutturale su campioni minimi) un arsenale di tecniche trasferibili. E viceversa, la comprensione della mineralogia da impatto potrebbe fornire un quadro di riferimento per interpretare le fasi ancora non identificate nella trinitite.
Il clatrato come marker chimico dell’evento
C’è un’ultima prospettiva che merita attenzione, non strettamente legata alle proprietà materiali ma alla chimica forense e alla fisica storica. Il fatto che il clatrato Ca–Cu–Si si trovi nelle immediate vicinanze del quasicristallo, entrambi all’interno delle stesse goccioline di rame nella trinitite rossa, permette di ricostruire con maggiore precisione le condizioni locali dell’esplosione del 1945.
La composizione chimica di queste microstrutture riflette la miscela di materiali presenti nell’istante della detonazione: il rame dei cavi, il silicio della sabbia, il calcio probabilmente proveniente da minerali argillosi del suolo. La temperatura necessaria per fondere e miscelare questi elementi in modo omogeneo (necessaria perché si formi una struttura come quella del clatrato durante il raffreddamento) pone un vincolo termodinamico che può essere confrontato con i modelli idrodinamici dell’esplosione. È, in un certo senso, un termometro congelato nel vetro del deserto.
Questa funzione di “marker termodinamico” potrebbe essere utile anche in altri contesti: siti di fulminazione (la fulgurite contiene strutture amorfe e cristalline anomale), zone di impatto meteoritico poco studiate, o residui di altri test nucleari atmosferici. La trinitite non è l’unico vetro da esplosione nucleare esistente: test successivi nel Pacifico e nel Nevada hanno prodotto materiali analoghi, meno famosi e meno studiati. La metodologia sviluppata dal gruppo di Bindi apre la strada a un’analisi sistematica di questi materiali, che potrebbe rivelare ulteriori fasi non ancora identificate.
La struttura Ca–Cu–Si della trinitite rimarrà probabilmente un unicum per molto tempo ancora, un composto nato da un evento che nessun laboratorio intende replicare. Ma proprio per questo, la sua esistenza è una prova concreta che lo spazio dei possibili composti cristallini è molto più vasto di quanto i database attuali lascino supporre. Alcune strutture aspettano semplicemente le condizioni giuste per formarsi: condizioni che, nella maggior parte dei casi, la natura non fornisce mai, ma che un’esplosione nucleare ha prodotto, per un istante, nel deserto del New Mexico.
